Les défis de l’utilisation de l’imagerie pour l’étude du cancer
Résolution temporelle et spatiale optimale
La recherche sur les traitements du cancer nécessite souvent la combinaison de la microscopie à fluorescence et d’essais fonctionnels innovants. Grâce à une résolution temporelle et spatiale optimale, les chercheurs sont en mesure de suivre des événements dynamiques dans les cellules vivantes, tels que la migration cellulaire et les métastases. Ces processus dynamiques figurent au cœur du développement du cancer.
L’imagerie rapide sur des périodes prolongées
La compréhension de ces processus a été difficile en raison de la difficulté d’observer le comportement des cellules tumorales en temps réel. L’imagerie rapide sur des périodes prolongées tend à s’accompagner d’un sacrifice : soit une résolution réduite, soit, plus souvent, un préjudice pour vos précieux échantillons. Le défi consiste à trouver la technique et le système d’imagerie capables de fournir les meilleures données avec la plus haute résolution tout en maintenant les cellules en vie afin que vous puissiez suivre les processus qui vous intéressent.
Articles connexes
Empowering Spatial Biology with Open Multiplexing and Cell DIVE
AI-Powered Multiplexed Image Analysis to Explore Colon Adenocarcinoma
A Meta-cancer Analysis of the Tumor Spatial Microenvironment
Spatial Architecture of Tumor and Immune Cells in Tumor Tissues
Le multiplexage pour comprendre les mécanismes de la maladie
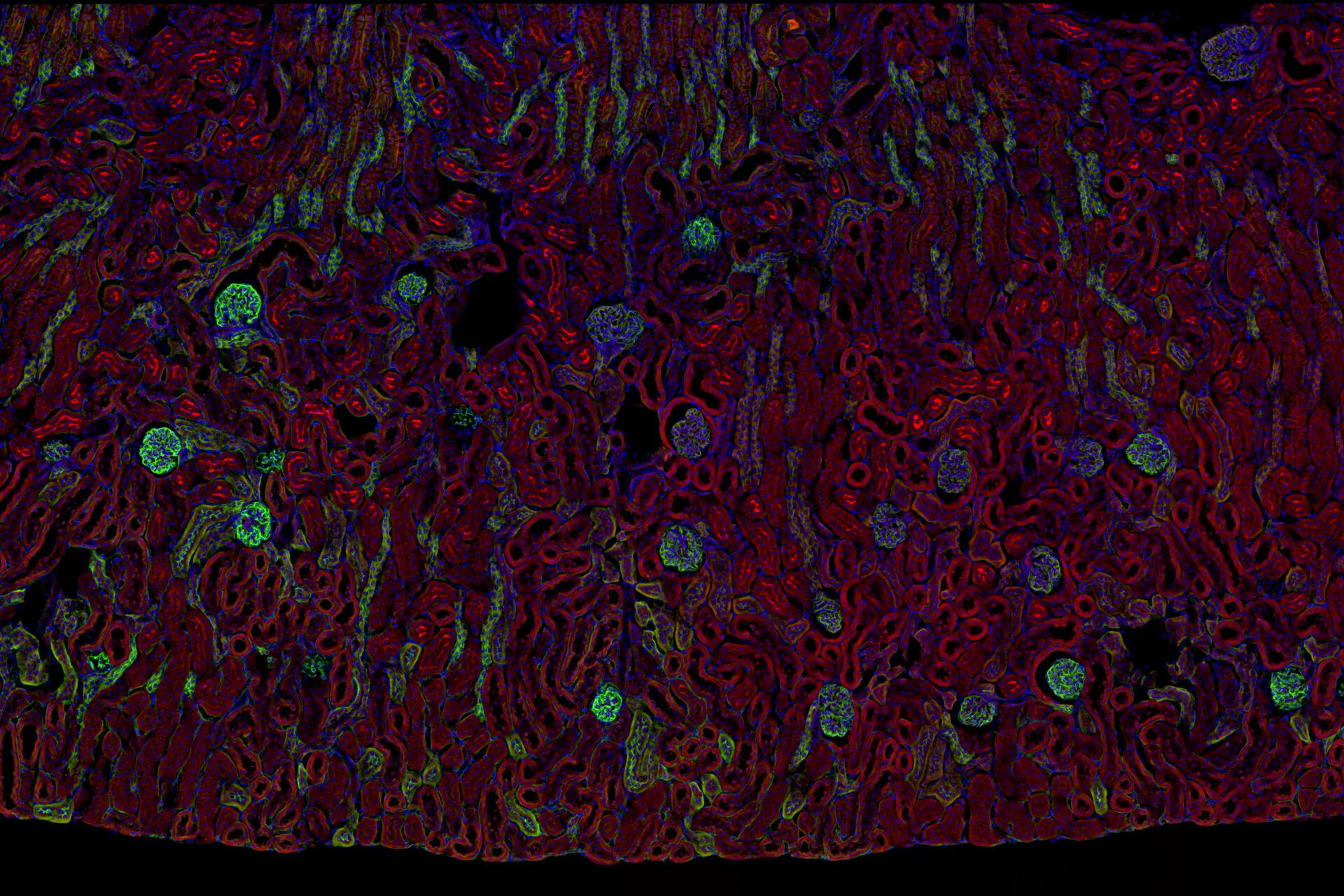
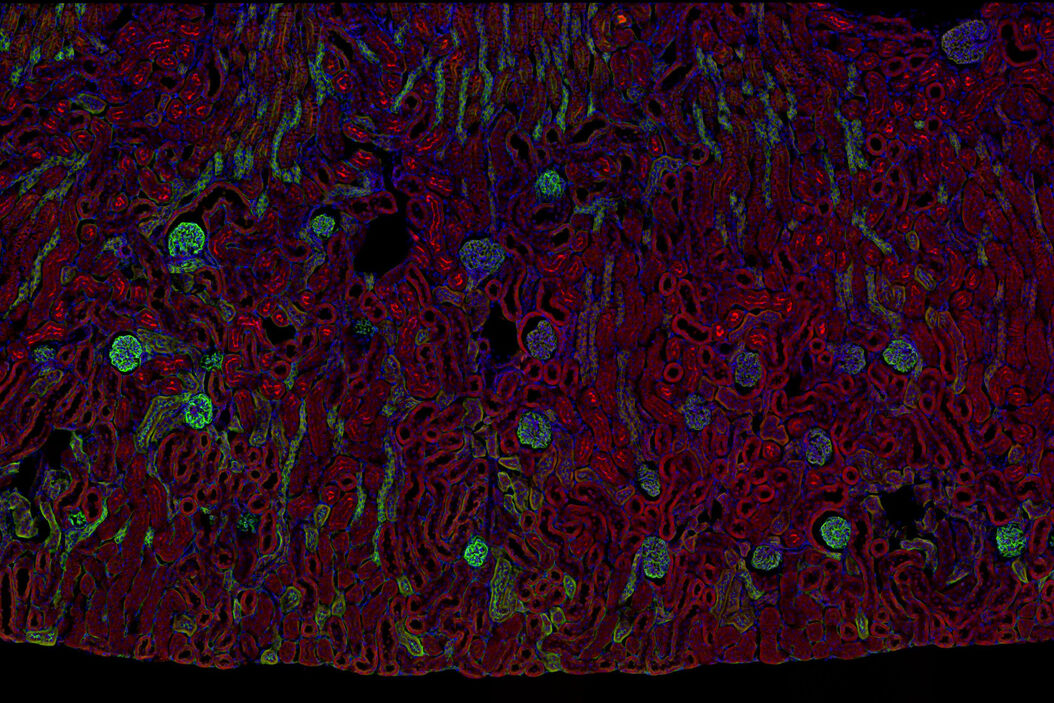
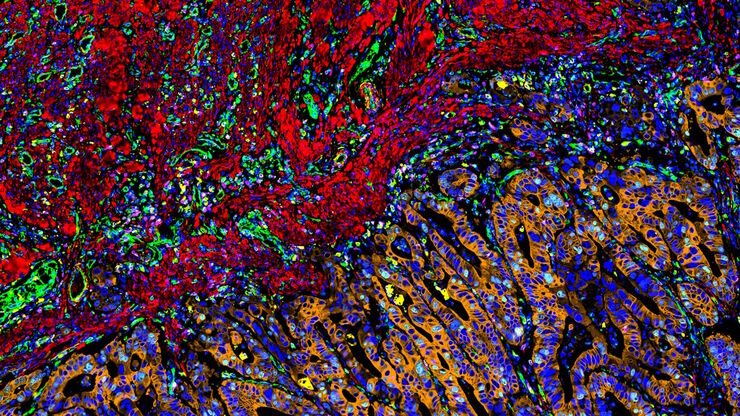
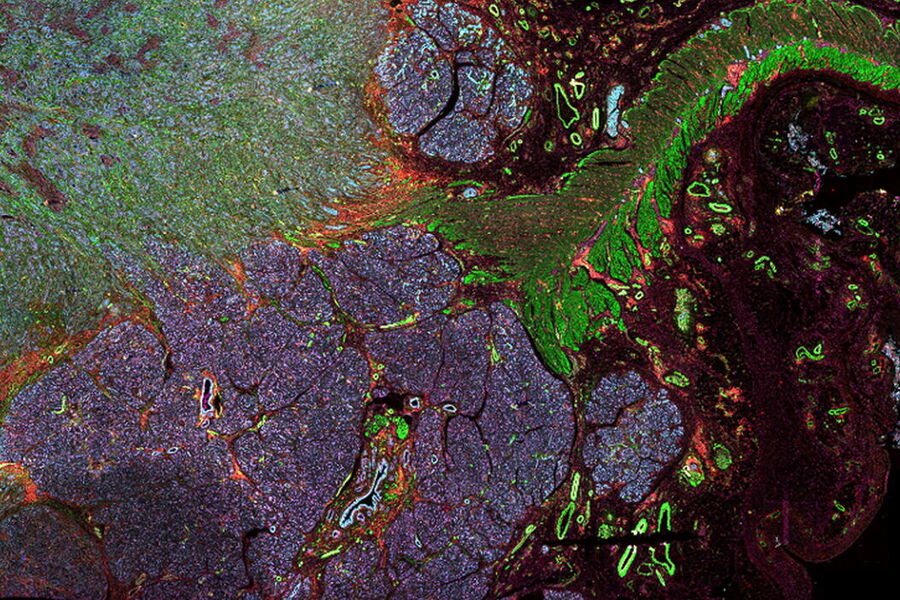
La microscopie à fluorescence multicouleur, qu’elle soit confocale ou à champ large, est un outil fondamental pour comprendre le contexte spatial, la colocalisation et la proximité de biomarqueurs multiples lors de l’étude d’événements complexes, tels que l’immunosuppression ou l’angiogenèse. Cet objectif peut souvent s’avérer difficile à atteindre, car il y a des limites au nombre de fluorophores que l’on peut distinguer efficacement grâce à cette approche de « multiplexage ». Heureusement, il existe des systèmes et des stratégies d’imagerie innovants permettant d’améliorer la séparation des fluorophores (par exemple, FluoSync - une approche rationalisée pour l’imagerie fluorescente multiplexe simultanée à l’aide d’une seule exposition) et d’augmenter le nombre de sondes fluorescentes en fonction des besoins de votre expérience.
Trouver les bons outils
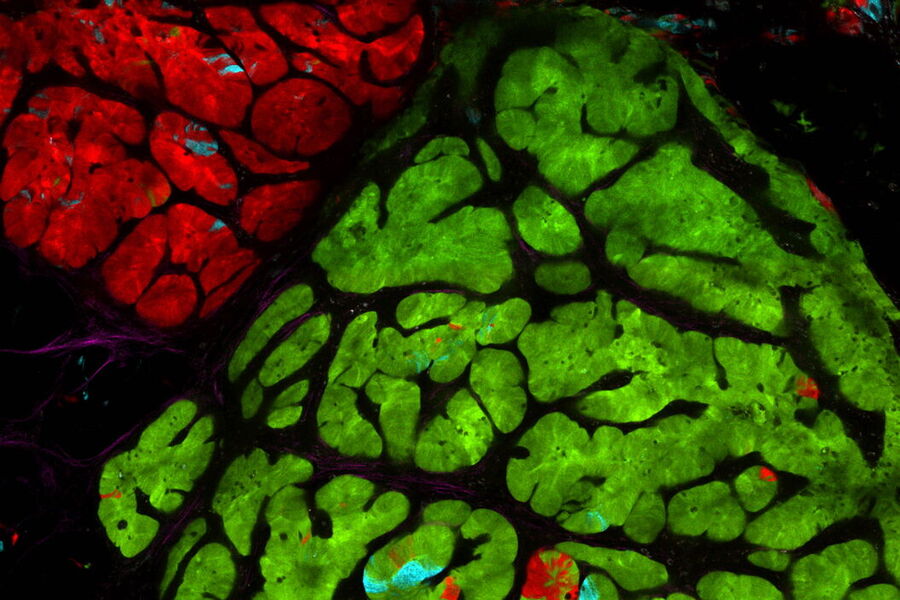
Le cancer est une maladie complexe qui nécessite une myriade de méthodes, dont l’imagerie à résolution spatiotemporelle, l’imagerie sur échantillon vivant et l’imagerie monocellulaire. Les méthodes d’analyse d’images multiparamétriques et de résolution la plus élevée possible permettront probablement de mieux comprendre les processus cellulaires liés au cancer. Des approches comme la microscopie confocale à fluorescence permettent d’étudier de multiples cibles dans les tissus ou les structures cellulaires.
Les techniques d’imagerie avancées, telles que l’imagerie de super-résolution ou, plus récemment, l’imagerie en temps de vie ou le light sheet, vous aident à mieux comprendre les interactions moléculaires et les mécanismes de régulation à l’origine de l’apparition et de la progression des tumeurs, ainsi que la réponse au traitement.
La microdissection laser ou la microscopie optique et électronique corrélative (CLEM) permettent d’étudier l’agencement spatial des récepteurs dans les membranes et l’organisation du génome dans les noyaux cellulaires.
Microscopes à super-résolution et nanoscopes
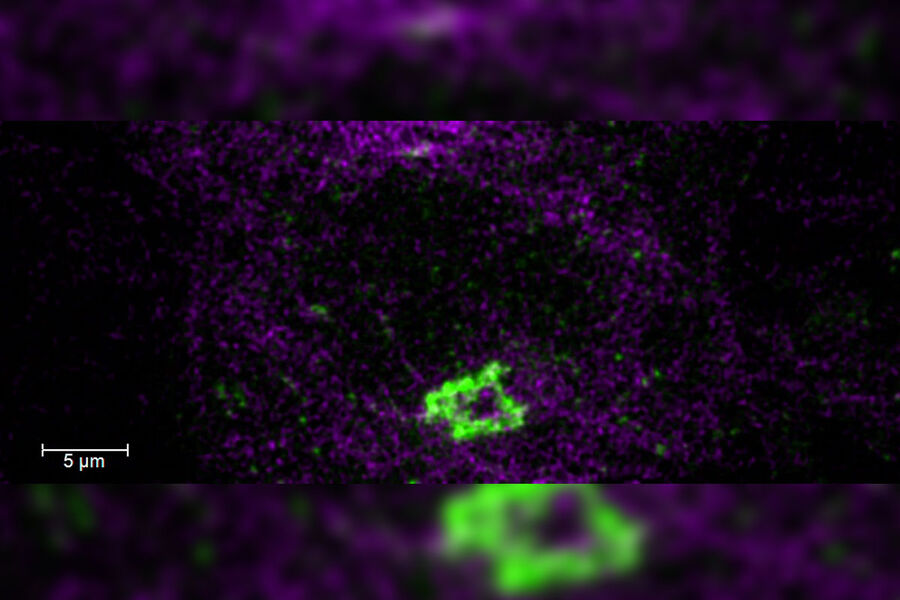
Les microscopes à super-résolution et nanoscopes dépassent la limite de diffraction de la lumière et permettent aux chercheurs d'examiner les structures subcellulaires plus en détail par rapport à ce que permet un microscope confocal standard. La technique STED permettant d'atteindre des résolutions de 30 nm , il est désormais possible d'étudier la morphologie ainsi que la dynamique subcellulaire à l'échelle du nanomètre.
Microscopie Fluorescente
La fluorescence est l'un des phénomènes physiques les plus couramment utilisés en microscopie biologique et analytique, principalement en raison de sa grande sensibilité et de sa haute spécificité. Découvrez comment les microscopes à fluorescence appuient votre recherche.
L’imagerie en temps de vie de fluorescence
La microscopie en temps de vie de fluorescence (FLIM) désigne une technique d’imagerie qui utilise les propriétés inhérentes des colorants fluorescents. Chaque molécule fluorescente présente non seulement des spectres d’émission caractéristiques, mais aussi une durée de vie propre qui reflète le temps que le fluorophore passe à l’état excité avant d’émettre un photon. L’analyse de la durée de vie fournit des informations venant compléter les mesures standard de l’intensité de la fluorescence.