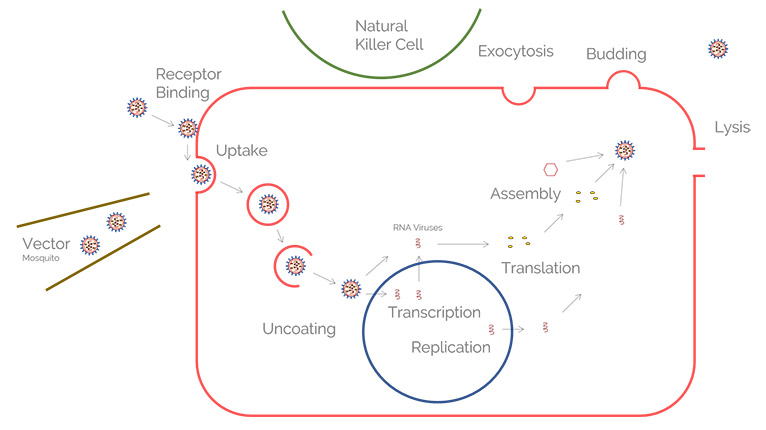
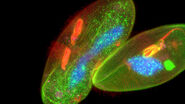
ウイルス感染過程の宿主側
ウイルス研究ではモデル生物が用いられることもありますが、ヒトの宿主の形態をうまく模倣することはできません。 このため、研究者はヒト細胞、生体検査、細胞培養研究に頼ることが多くなります。
生体外感染モデルは組織、生体検査、動物モデルから生成することができます。 ライカ実体顕微鏡はこのようなモデル研究に効果的です。
ライカのワイドフィールド顕微鏡を使用することで、細胞培養、スフェロイド、オルガノイドをモニタリングすることが可能です。
THUNDERイメージャーといったライカの蛍光顕微鏡を活用して、感染モデル、2Dまたは3D細胞培養の初期研究をさらに深めることができます。
特定の細胞を周囲組織から分離する、ライカマイクロシステムズのレーザーマイクロダイセクションによって、より確かな遺伝子分析を実施できます。
ライカソリューションのウイルス研究アプリケーションはこちらのアプリケーションノートでご覧いただけます。
関連記事
Microscopy in Virology
How to Sanitize a Microscope
ウイルス研究のための高分解能蛍光イメージング
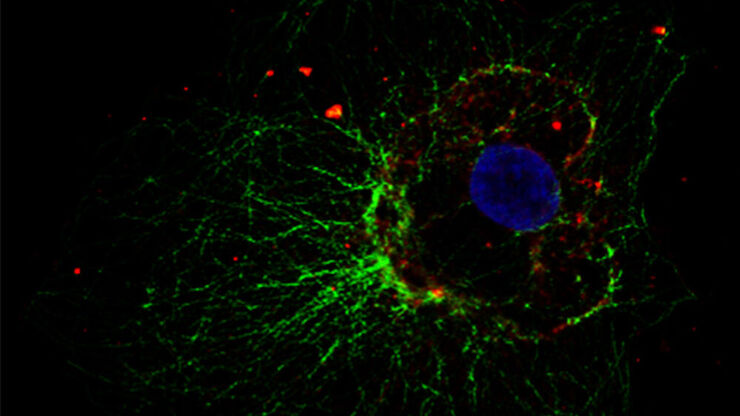
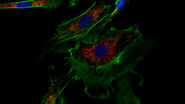
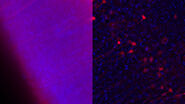
原因となるウイルスや病原体を追跡することを可能にする高分解能顕微鏡観察は、感染症研究にとって有用です。 細胞やウイルス成分の蛍光標識と組み合わせることで、感染過程の複数の側面を研究することができます。
このため、超高分解能を得る共焦点レーザー顕微鏡と全反射照明蛍光(TIRF)顕微鏡は、共にウイルス研究に最適なツールです。
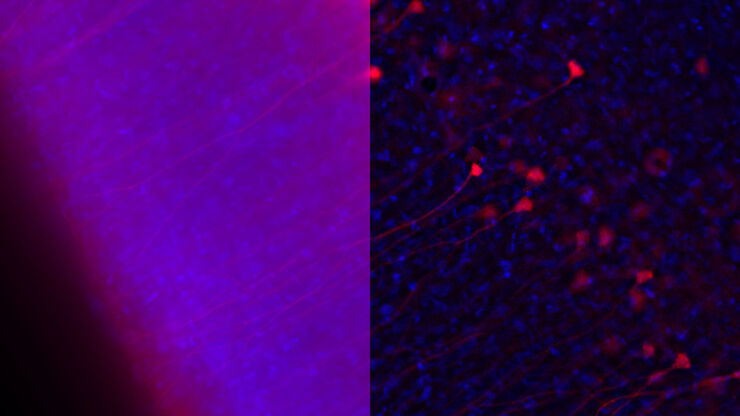
多光子とライトシートによる顕微鏡観察といった高度な顕微鏡技術は、組織切片、動物モデル、オルガノイド等の3D感染モデルといった異なる状況下で発生する感染事例にアクセスすることを可能にします。
STELLARIS共焦点プラットフォームとTIRF ソリューションを含むライカの顕微鏡は、ウイルス研究に関連した3D試料の研究にとって多くの利点を提供します。
画像および図表出典:Coomer et al. PLOS Pathogen (2020) 16(2): e1008359, DOI: 10.1371/journal.ppat.1008359.

関連記事
Introduction to Fluorescent Proteins
How to Prepare your Specimen for Immunofluorescence Microscopy
Studying Virus Replication with Fluorescence Microscopy
How Can Immunofluorescence Aid Virology Research?
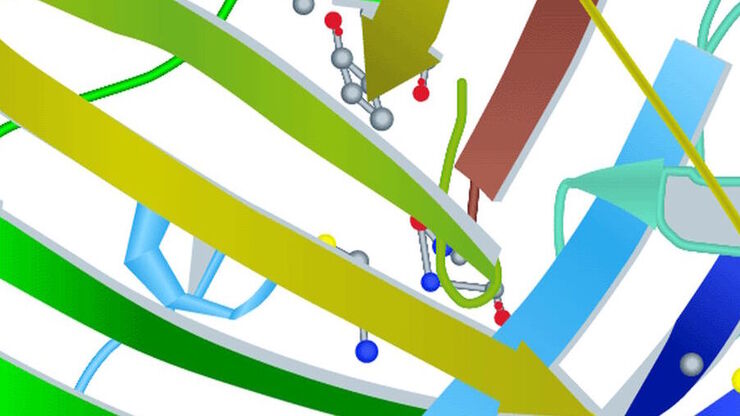
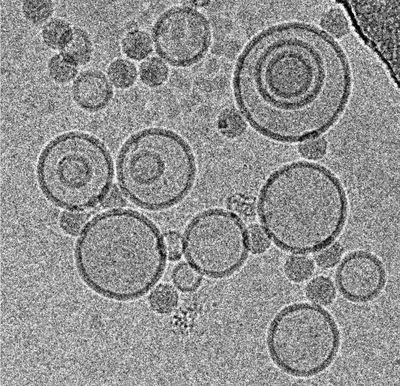
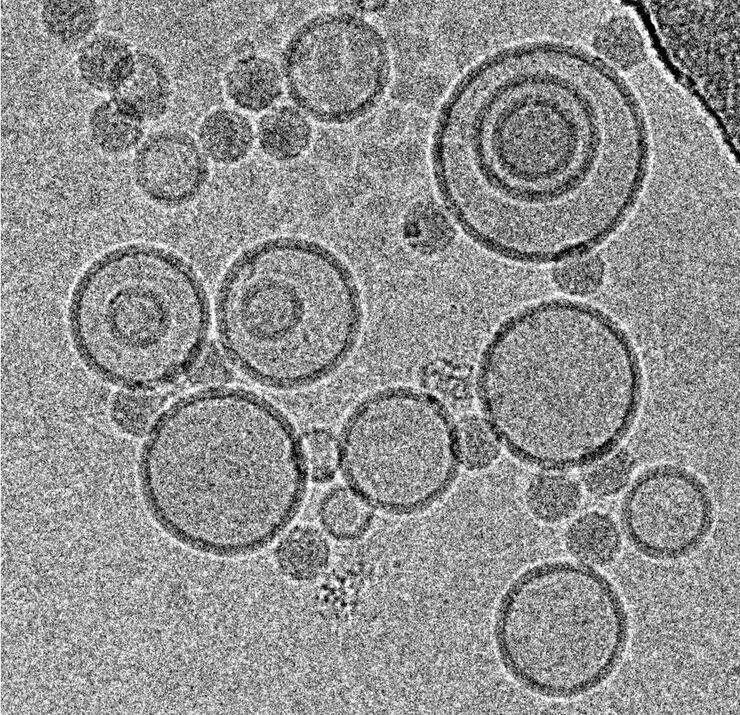
ウイルスの超微細構造
ウイルスの超微細構造の評価には、1 nm近い分解能が必要です。 現在、この分解能は電子顕微鏡によってのみ達成できます。 クライオ電子顕微鏡は、ナノメートル以下の分解能さえ達成できます。
超微細構造分解能は、宿主とウイルス間相互作用のナノスケールでの観察、異なる分析技術による結果の確認、薬物標的部位の特定を可能にします。 さらに、ウイルス粒子の相互作用時に標的となった細胞表面レセプターのリガンドや小分子は、ワクチンとウイルス侵入阻害剤の構造情報に基づいたデザインにとって鍵となります。
従来の電子顕微鏡やクライオ電子顕微鏡にとって、試料作製は極めて重要です。 ライカマイクロシステムズは、専門的な機器や知識が求められるこのプロセスを、電子顕微鏡試料作製の広範なポートフォリオでサポートします。さらに、ライカのエキスパートがアドバイスを提供します。